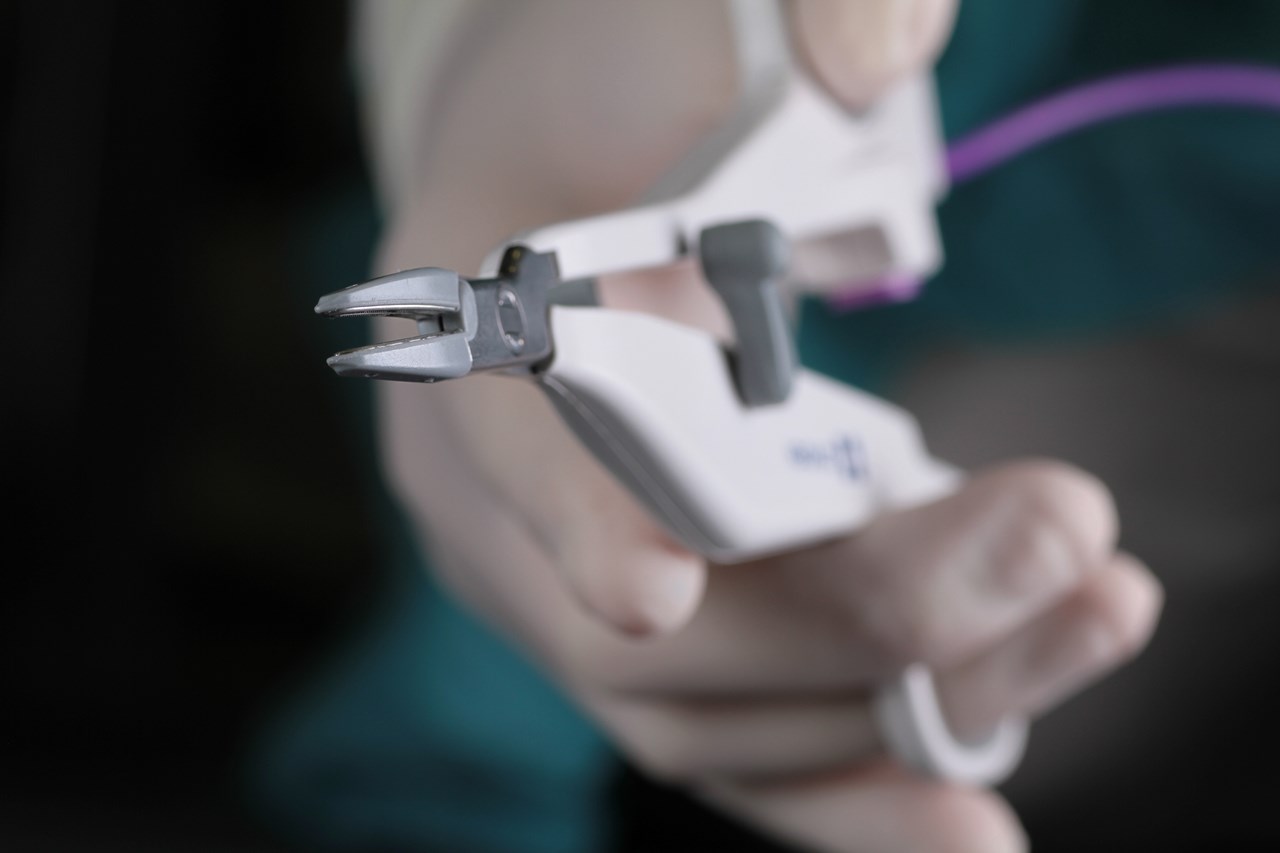
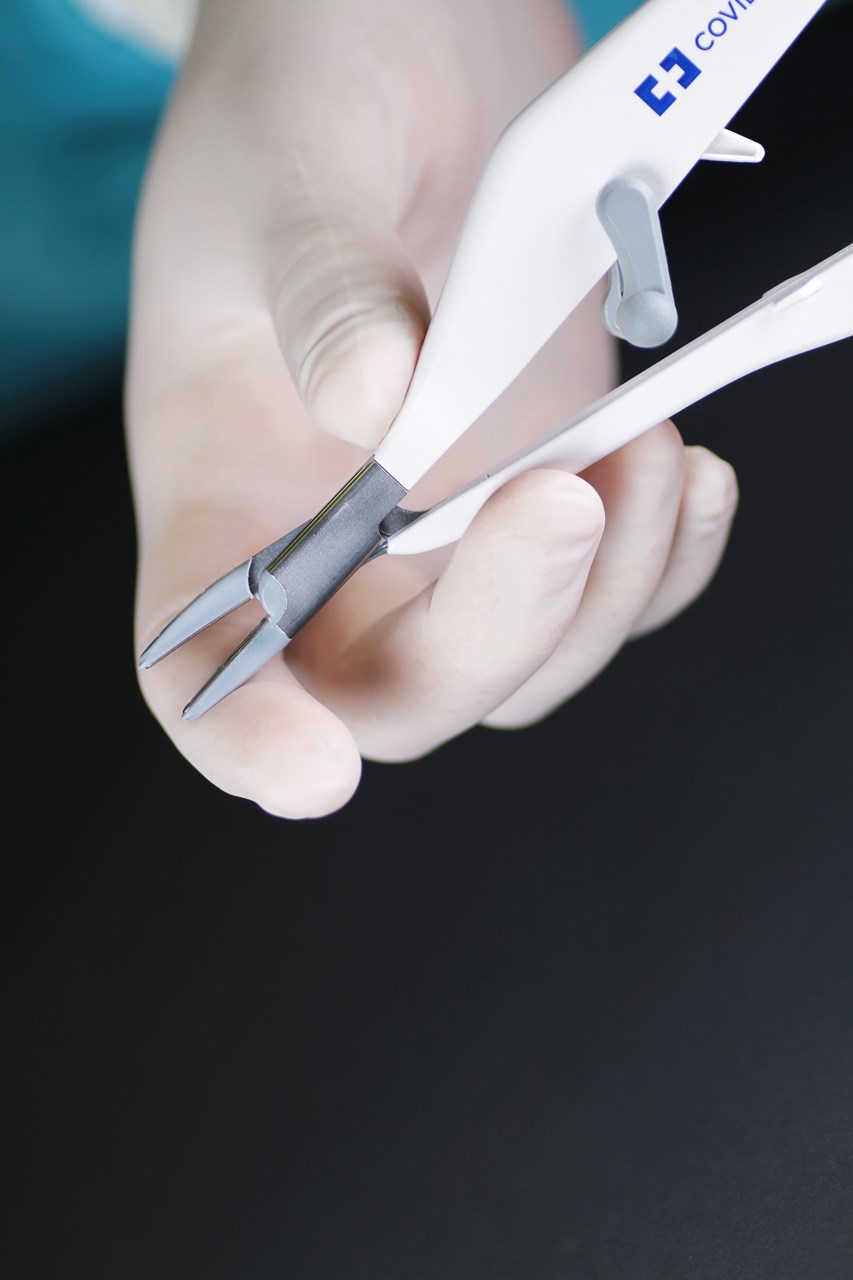
Tiroidectomía
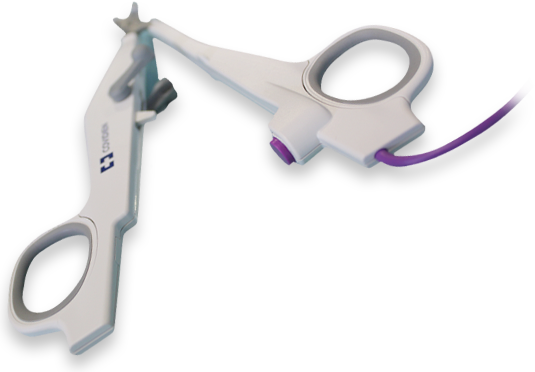
Aplicación del LigaSure™ Small Jaw Instrument
Resumen del programa
La finalidad de este módulo de e-learning es esbozar la energía bipolar avanzada del LigaSure™ Small Jaw Instrument, que se emplea durante las tiroidectomías para el tratamiento de enfermedades tiroideas.
En el módulo en línea de 25 minutos, se revisarán los principios básicos de la energía bipolar avanzada; las técnicas quirúrgicas y recomendaciones para un uso seguro y eficaz; y la investigación basada en la evidencia del uso del LigaSure™ Small Jaw Instrument en pacientes sometidos a tiroidectomía en relación al tiempo operatorio, la pérdida de sangre y el alta del paciente.
Objetivos del programa
- Conocer la literatura clínica relativa al uso de la energía avanzada en la tiroidectomía.
- Aprender a identificar y orientar los problemas que habitualmente se encuentran al utilizar la energía avanzada en las tiroidectomías.
- Aprender a minimizar las complicaciones comunes del postoperatorio.
- Obtener consejos técnicos para el uso de la energía avanzada durante la tiroidectomía.


Fuentes De Energía
Energía avanzada
Leer más
- Butskiy O, Wiseman SM. Electrothermal bipolar vessel sealing system (LigaSure) for hemostasis during thyroid surgery: a comprehensive review. Expert Rev Med Devices 2013;10:389-410. PubMed
- Parmeggiani D, De Falco M, Avenia N, Sanguinetti A, Fiore A, Docimo G, Ambrosino P, Madonna I, Peltrini R, Parmeggiani U. Nerve sparing sutureless total thyroidectomy. Preliminary study Ann Ital Chir. 2012 ;83:91-6. PubMed
- Dionigi G, Boni L, Rausei S, Frattini F, Ferrari CC, Mangano A, Leotta A, Franchin M. The safety of energy-based devices in open thyroidectomy: a prospective, randomised study comparing the LigaSure (LF1212) and the Harmonic® FOCUS. Langenbecks Arch Surg. 2012;397:817-23. PubMed
- Rahbari R, Mathur A, Kitano M, Guerrero M, Shen WT, Duh QY, Clark OH, Kebebew E. Prospective randomized trial of ligasure versus harmonic hemostasis technique in thyroidectomy. Ann Surg Oncol. 2011;18:1023-7. PubMed
- Saint Marc O, Cogliandolo A, Piquard A, Famà F, Pidoto RR. LigaSure vs clamp-and-tie technique to achieve hemostasis in total thyroidectomy for benign multinodular goiter: a prospective randomized study. Arch Surg. 2007 Feb;142:150-6. PubMed
Strasbourg (FRANCE)
Profesor de Cirugía Digestiva y Endocrina
Hospital Universitario de Estrasburgo, Francia

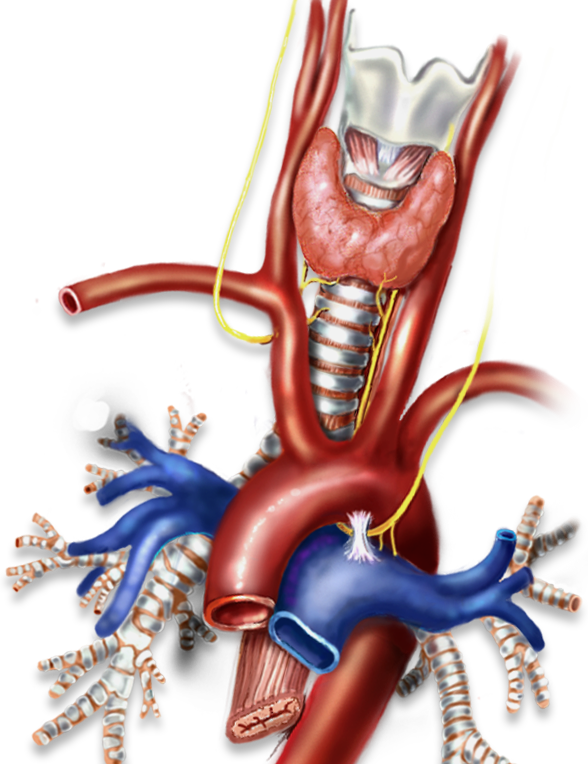
Técnica Quirúrgica

La descripción de la tiroidectomía mínimamente invasiva asistida por vídeo cubre todos los aspectos de la intervención quirúrgica que se emplea para el tratamiento de nódulos tiroideos.
Se describen minuciosamente la preparación del quirófano, la posición del paciente y el equipamiento y el instrumental utilizados. Los principales puntos técnicos de la intervención quirúrgica se presentan paso a paso: disección, ligaduras, y extracción o resección.
Todo ello hace que la técnica quirúrgica de esta patología sea una técnica normalizada.
Strasbourg (FRANCE)
Cirujano Digestivo y Endocrino
Hospital Universitario de Estrasburgo, Francia

- 1. IntroducciónDesde la primera publicación de una paratiroidectomía endoscópica (Gagner, 1996), las técnicas asistidas por vídeo se han aplicado a la cirugía del cuello. Varias series (Miccoli y col., 2000; Henry y col., 1999) han documentado la idoneidad de este abordaje en la patología paratiroidea y tiroidea. Las primeras intervenciones endoscópicas para la resección de pequeños nódulos tiroideos se practicaron en 1998 (Miccoli y col., 2001a; Ohgami y col., 2000; Shimizu y col., 1999). Estas intervenciones no se han popularizado porque las ventajas de este tipo de cirugía mínimamente invasiva son menos evidentes que en la cirugía abdominal. Esto es particularmente cierto en el caso de la tiroidectomía, para la que existe un procedimiento abierto normalizado. La principal desventaja de estas intervenciones mínimamente invasivas reside en el escaso número de pacientes a los que pueden beneficiar, especialmente en zonas de bocio endémico. Asimismo, se espera que inicialmente, los tiempos operatorios y las tasas de complicaciones sean más altos, al igual que en cualquier nueva intervención mínimamente invasiva. Los costes y las lagunas tecnológicas también pueden disuadir del uso de estas técnicas. La cirugía de tiroides está muy extendida. En este capítulo se describe una técnica quirúrgica convencional y normalizada, con unos riesgos mínimos para las paratiroides y el recurrente. Es una técnica segura y reproducible en la mayoría de casos. La técnica ha sido adaptada y personalizada de acuerdo con los principios de Charles Proye. El uso de medios hemostáticos modernos posibilita la reducción del tiempo operatorio y la prevención de posibles riesgos. Esta técnica se puede emplear en todo tipo de patología tiroidea, benigna o maligna.
- 2. Anatomía
- • Embriología1. Primer saco faríngeo
2. Segundo saco faríngeo
3. Cordón epitelial
4. Glándula tiroides
La glándula tiroides comienza a formarse alrededor del 17º día de desarrollo, entre el primer y el segundo saco faríngeo. Rápidamente, el primordio glandular forma un cordón epitelial que penetra en el suelo de la cavidad oral y, al perder su conexión con el suelo faríngeo, alcanza la cara anterior de la tráquea.
En este momento, la punta del ducto se bifurca y posteriormente se expande en sentido transversal en 2 lóbulos laterales. En algunos casos, el ducto puede persistir parcialmente en forma de quiste tirogloso.
- • Anatomía quirúrgica1. Lóbulo derecho
2. Lóbulo izquierdo
3. Istmo
4. Lóbulo piramidal
5. Cápsula
6. Ligamento de Berry
7. Músculo esternotiroideo
8. Músculo esternohioideo
La glándula tiroides consta de 2 lóbulos unidos por un istmo. El peso normal de una glándula adulta es de unos 20 g. Cada lóbulo tiene una forma cónica y mide unos 2 x 3 x 5 cm. Un tiroides normal es de color rojo vinoso oscuro, blando y está recubierto por una fina cápsula.
La glándula está situada en la parte inferior del cuello y su istmo cruza la tráquea a nivel del segundo y tercer anillos traqueales. El ligamento suspensorio posterior (ligamento de Berry) une la glándula a su estructura.
La glándula está cubierta por los músculos infrahihoideos (músculos esternohioideo y esternotiroideo), unidos en la línea media por la línea alba cervical (fascia cervical anterior). La cara medial de cada lóbulo descansa sobre la laringe y la tráquea. El esófago está situado en la cara posteromedial del lóbulo tiroideo y el nervio recurrente discurre más o menos verticalmente a lo largo del canal traqueoesofágico. Los polos superiores están en contacto con el músculo constrictor inferior y la cara posterior del músculo cricotiroideo. Normalmente, el polo inferior alcanza el cuarto o quinto anillo traqueal. Frecuentemente, un remanente del conducto tirogloso se extiende desde el istmo en sentido craneal, y su grado de desarrollo es variable (lóbulo piramidal). - • Irrigación sanguínea1. Arteria carótida externa
2. Arteria tiroidea superior
3. Nervio laríngeo superior
4. Arteria tiroidea inferior
5. Tronco tirocervical
6. Nervio laríngeo inferior
7. Glándula paratiroides inferior
8. Glándula paratiroides superior
9. Vena tiroidea superior
10. Vena tiroidea media
11. Vena tiroidea inferior
La glándula recibe el riego sanguíneo arterial de las arterias tiroideas superior e inferior. La arteria tiroidea superior se origina en la arteria carótida externa. Desciende junto a la superficie del constrictor inferior de la faringe y se introduce en el polo superior del tiroides por su superficie anterosuperior. En aproximadamente el 10% de los casos, una rama de esta arteria irriga la glándula paratiroides superior. La rama externa del nervio laríngeo superior discurre muy cerca de las ramas de la arteria tiroidea superior, aunque su relación varía bastante.
La arteria tiroidea inferior es una rama del tronco tirocervical; discurre por detrás de la arteria carótida común y de la vena yugular hacia el cartílago cricoides. A nivel de la glándula, la arteria se curva en sentido descendente y medial, y se introduce en el área medial del lóbulo, dividiéndose en diversas ramas terminales. Esta arteria y sus ramas mantienen una estrecha relación con el nervio laríngeo inferior. Una rama de la arteria tiroidea inferior habitualmente irriga la glándula paratiroides inferior; en la mayoría de casos, la arteria tiroidea inferior irriga también la glándula paratiroides superior. En raras ocasiones, está presente una arteria tiroidea (arteria tiroidea ima): nace del tronco braquiocefálico y se introduce en el istmo.
El drenaje venoso es más variable que el riego arterial. La vena tiroidea superior está estrechamente relacionada con la arteria tiroidea superior y drena en la vena yugular interna. El número de venas tiroideas medias es variable y estas discurren por el borde lateral del lóbulo hacia la vena yugular. Las venas inferiores están separadas de las arterias tiroideas inferiores y drenan la sangre de los lóbulos inferiores en las venas yugular interna o braquiocefálica. - • Drenaje linfático1. Compartimento central
2. Compartimento lateral
3. Vena braquiocefálica
4. Tráquea
5. Carótida
El drenaje linfático de la glándula tiroides es muy extenso. El cirujano debe tomar en consideración 2 zonas principales de drenaje linfático: el compartimento central (espacio periglandular) y el compartimento lateral. La hoja carotidea separa los 2 compartimentos.
El compartimento central incluye los grupos prelaríngeo, pretraqueal y paratraqueal-esofágico. Los músculos infrahioideos constituyen el límite anterior de este compartimento. Existe una amplia conexión entre los 2 compartimentos y los 2 lados, debido a la existencia de una red capsular, que se comunica con los vasos linfáticos profundos. Inferiormente, el compartimento central está delimitado por la vena braquiocefálica, medialmente por la tráquea y lateralmente por la carótida. - • Nervios laríngeos
- • Superior1. Nervio laríngeo superior
2. Polo tiroideo superior
3. Músculo constrictor medio
4. Rama externa del nervio laríngeo superior
5. Rama interna del nervio laríngeo superior
6. Músculo cricotiroideo
La rama externa del nervio laríngeo superior está en íntimo contacto con los vasos tiroideos superiores y el polo superior del tiroides. El nervio laríngeo superior nace en el nervio vago y desciende, para finalizar en los músculos constrictores medios. A este nivel, se divide en sus ramas externa e interna. La rama externa continúa su trayecto en sentido inferior e inerva el músculo cricotiroideo. Este músculo produce la tensión de la cuerda vocal; las lesiones de la rama externa pueden, por tanto, comprometer los sonidos vocales agudos. En el 6% al 18% de los casos (Berti y col., 2002), la rama externa del nervio laríngeo superior discurre junto con o alrededor de la arteria tiroidea superior o sus ramas, por lo que es susceptible de ser lesionado durante la disección quirúrgica. En casi un 20% de los casos (Berti y col., 2002), no está situado en el área accesible quirúrgicamente de alrededor del polo superior de la glándula tiroides y durante la cirugía convencional no puede visualizarse; con el endoscopio, una magnificación óptica y un ángulo de 30° permiten exponer toda la superficie anterior del músculo cricotiroideo. Así, su preparación se logra fácilmente en las intervenciones asistidas por vídeo; en caso de que su curso imposibilite su visualización, la arteria tiroidea superior se deberá ligar selectivamente muy cerca de la cápsula del tiroides. - • Inferior1. Nervio laríngeo inferior
2. Nervio vago
3. Arteria subclavia derecha
4. Cayado aórtico
El nervio laríngeo inferior nace en el nervio vago e inerva todos los músculos de la laringe, excepto el músculo cricotiroideo. Por el lado derecho, el nervio rodea posteriormente la arteria subclavia. Por el lado izquierdo, el nervio pasa alrededor del cayado aórtico. Ambos nervios tienen un recorrido craneal y medial hacia el cartílago cricoides, donde penetran en la laringe. El nervio laríngeo inferior no es un único nervio, sino que se divide en varias ramas (hacia el esófago, la tráquea y el tiroides), y se anastomosa con otras estructuras nerviosas (nervio laríngeo superior, sistema simpático, nervio contralateral). La relación entre la arteria tiroidea inferior y el nervio laríngeo inferior es muy variable. Este último puede transcurrir en posición anterior, posterior o entre las ramas de la arteria. En menos de un 1% de los casos (Henry y col., 1988), el nervio no transcurre por el lado derecho y se origina directamente en el vago a nivel del cuello, alcanzando la laringe tras un recorrido más o menos transversal. Esta variación viene determinada por una anomalía vascular durante el desarrollo embrionario, que da lugar a una arteria subclavia aberrante (la arteria lusoria), que nace directamente en el cayado aórtico, a la izquierda de la arteria subclavia izquierda, y tiene un recorrido posterior y transversal hasta el esófago. Esta anomalía es excepcional en el lado izquierdo y ocurre en casos de situs inversus visceral con anomalía vascular asociada. - 3. IndicacionesLa tiroidectomía convencional sigue siendo el modelo de referencia para el tratamiento de la mayor parte de patologías benignas o malignas de tiroides. Las técnicas mínimamente invasivas permiten tratar patologías bien orientadas y no pueden emplearse en todos los casos.
- 4. Periodo preoperatorioRequisitos principales
Análisis de sangre: para controlar las concentraciones de hormonas tiroideas y detectar una posible tiroiditis.
Ecografía: para evaluar el volumen glandular y la posible presencia de ganglios linfáticos sospechosos.
Biopsia-aspiración con aguja fina (BAAF): para evaluar el tipo de nódulo (benigno, maligno, sospechoso). - 5. Preparación del quirófano
- • Paciente- en posición supina con hiperextensión del cuello;
- preparación del cuello y recubrimiento convencionales;
- una talla estéril para recubrir el cuello. - • Equipo1. El cirujano está de pie a la derecha del paciente.
2. El primer ayudante está de pie frente al cirujano.
3. El segundo ayudante está de pie a la derecha del cirujano.
4. El instrumentista se sitúa a la izquierda del primer ayudante, frente al cirujano. - • EquipamientoEl equipamiento necesario es el siguiente:
1. Mesa de operaciones
2. Equipamiento anestésico
3. Electrocauterizador
4. LigaSure™ Precise Small Jaw
No se precisa ecógrafo. - 6. Instrumental1. Dos pinzas de sujeción
2. Dos pinzas estándar
3. Una pinza hemostática
4. Electrocauterizador o escalpelo eléctrico
5. Un LigaSure™ Precise Small Jaw
6. Una pinza angulada a la derecha
7. Un par de tijeras
8. Un aplicador de grapas
9. Suturas para la suspensión del colgajo
10. Cuatro retractores de Farabeuf
11. Dos retractores de Langenbeck
12. Dos pinzas de tracción atraumática
13. Un porta agujas
14. Una pinza de Kelly - 7. Disección de la glándula tiroides
- • Preparación del cuello
- • Incisión cutáneaSe practica una incisión adaptada al tamaño de la lesión, 2 cm por encima de la hendidura esternal. Se corta el tejido subcutáneo.
- • Disección del tejido subcutáneo
- • Suspensión del colgajo de pielSe diseca un colgajo de la piel superior mediante electrocauterización. Se tracciona sobre este colgajo para lograr una exposición adecuada de la región cervical.
- • Apertura del canal yugulocarotideo
- • Disección del músculo ECMSe diseca el borde interno del músculo esternocleidomastoideo (ECM) con el fin de esqueletizar la cara anterior de la vena yugular.
- • Disección del músculo omohioideoSe diseca el borde interno del músculo omohioideo.
- • División de la vena media
- 8. Lóbulo derecho
- • Identificación de la arteria tiroidea inferior y del nervio recurrenteSe diseca el espacio situado entre el paquete vascular yugular y carotideo y la glándula tiroides. Los retractores colocados sobre la arteria carótida y la glándula tiroides permiten esqueletizar la arteria tiroidea inferior y buscar el nervio recurrente.
- • División de los músculos pretiroideosCuando se han identificado estas dos estructuras musculares, se dividen utilizando el LigaSure™ Precise Small Jaw.
- • Disección del polo superior
- • Disección del polo superiorLuego se aborda el polo superior de la glándula. Las caras anterior y lateral de la glándula tiroides se disecan para separarlas de los músculos pretiroideos.
- • División de los vasos del polo superiorSe disecan y se dividen los vasos del polo superior.
- • Disección del lóbulo superior derechoSe identifica el nervio laríngeo superior y se protege. Los vasos del polo superior se dividen utilizando el LigaSure™ Precise Small Jaw.
- • Disección del polo inferior de la glándulaA continuación se accede polo inferior de la glándula. Los vasos se disecan y se dividen.
- • Disección de las paratiroides
- • Disección de la glándula paratiroides inferiorLuego puede retraerse la glándula tiroides para exponer su cara lateral. Se buscan las glándulas paratiroides y se hacen descender. La glándula paratiroides inferior se buscará en la zona anterior a la unión de la arteria y el nervio. Si no se encuentra en posición ortotópica, se buscará en la parte posterosuperior del canal tirotímico.
- • Disección de la glándula paratiroides superiorLa glándula paratiroides superior se encuentra en la inserción superior de la rama de la arteria tiroidea superior.
- • Finalización de la disección de la glándula
- • Descenso del nervio laríngeo
- • Liberación del lóbulo derecho
- 9. Lóbulo izquierdo
- • Disección del polo superior
- • Disección vascular y nerviosa
- • Liberación del polo superior
- • Disección lateral
- • Disección de la arteria tiroidea inferior y el nervio recurrente
- • Disección del nervio recurrenteA continuación se diseca el nervio recurrente para hacerlo descender. El lóbulo se puede separar del lóbulo contralateral utilizando el LigaSure™ Precise Small Jaw.
En caso de tiroidectomía total, se repiten los mismos pasos y en el mismo orden cronológico. - 10. Resección de la glándula tiroides y cierre de la herida
- • Finalización de la disección
- • Drenaje y cierre del colgajo
- 11. ConclusiónSe trata de una técnica quirúrgica convencional y puede utilizarse en todas las patologías tiroideas. Los diferentes principios para la disección de ganglios linfáticos en caso de cáncer de tiroides no se describen. De igual modo, en caso de un bocio voluminoso o incluso profundo, la técnica deberá adaptarse dependiendo de la masa y de la posición del bocio.
- 12. Referencias bibliográficasBertt P. Materazzi G, Conte M, Galleri D, Miccoli P. Visualization of the external branch of the superior laryngeal nerve during video-assisted thyroidectomy. J Am Coll Surg 2002; 195:573-4. pubmed
Dralle H, Damm l, Scheumann GF, Kotzerke J, Kupsch E, Geerlings H et al. Compartment-oriented microdissection of regional lymph nodes in medullary thyroid carcinoma. Surg Today 1994:24:112-21. pubmed
Gagner M. Endoscopic subtotal parathyroidectomy in patients with primary hyperparathyroidism. Br J Surg 1996,83:875. pubmed
Henry JF, Audiffret J, Denizot A, Plan M. The nonrecurrent inferior laryngeal nerve: review of 33 cases, including two on the left side. Surgery 1988,104:977-84. pubmed
Henry JF, DeTechereux T, Gramatica L, de Boissezon C. Minimally invasive videoscopic parathyroidectomy by latéral approach. LangenbecksArch Surg 1999:384:298-301. pubmed
Miccoli P, Berti P, Raffaelli M, Conte M, Materazzi G, Galleri D. Minimally invasive video-assisted thyroidectomy. Am J Surg 2001 a; 181:567-70. pubmed
Miccoli P. Berti P, Raffaelli M, Materazzi G, Baldacci S, Rossi G. Comparison between minimally invasive video-assisted thyroidectomy and conventional thyroidectomy: a prospective randomized study. Surgery 2001b;130:1039-43. pubmed
Miccoli P. Bellantone R, Mourad M, Walz M, Raffaelli M, Berti P. Minimally Invasive Video-assisted Thyroidectomy: Multiinstitutional Experience. World J Surg 2002a;26:972-5. pubmed
Miccoli P. Elisei R, Materazzi G, Capezzone M, Galleri D, Pacini F et at. Minimally invasive video-assisted thyroidectomy for papillary carcinoma: a prospective study about its œmpleteness. Surgery, 2002b;132:1070-3; discussion 1073-4. pubmed
Miccoli P. Berti P, Conte M, Raffaelli M, Materazzi G'' Minimally invasive video-assisted parathyroidectomy: lesson learned from 137 cases. J Am Coll Surg 2000:191:613-8. pubmed
Ohgami M, Ishii S, Arisawa Y, Ohmori T, Noga K, Furukawa T et a/ Scariess endoscopic thyroidectomy: breis't approach for better cosmesis. Surg Laparosc Endosc Percutan Tech 2000; 10:1-4. pubmed
Shimizu K, Akira S, Jasmi AY, Kitamura Y, Kitagawa W, Akasu H et al. Video-assisted neck surgery: endoscopic resection of thyroid tumors with a very minimal neck wound. J Am Coll Surg 1999:188:697-703. pubmed
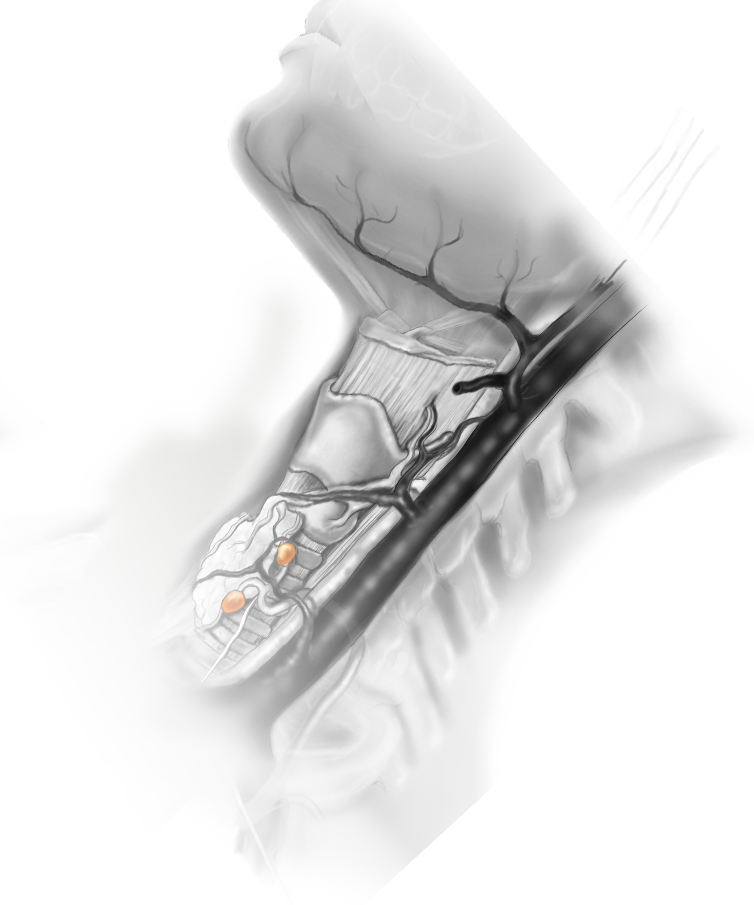
Opiniones De Los Expertos
Leer más
- Lepner U, Vaasnat T. Ligasure vessel sealing system versus conventional vessel ligation in thyroidectomy. Scand Journal Surg 2007:96;31-4. PubMed
- Covidien. Internal document. DSCHOW 7-5-12.
- Kim FJ, Chammas MF, Gewehr E, Morihisa M, Caldas F, Hayacibara E, Baptistussi M, Meyer F, Martins AC. Temperature safety profile of laparoscopic devices: Harmonic ACE (ACE), Ligature V (LV), and plasma trisector (PT). Surg Endosc 2008:22:1464-9. PubMed
- Scilletta B, Cavallaro MP, Ferlito F, Li Destri G, Minutolo V, Frezza EE, Di Cataldo A. Thyroid surgery without cut and tie: the use of Ligasure for total thyroidectomy. Int Surg 2010;95:293-8. PubMed
- Miccoli P, Davis T. Thyroid Surgery: Preventing and Managing Complications. Wiley-Blackwell Oxford 2013. Google Books
Profesor de Cirugía
Università degli Studi di Pisa, Italy

Strasbourg (FRANCE)
Profesora de Cirugía
Hospital Universitario de Estrasburgo


Intervención Quirúrgica
Paratiroidectomía
La cirugía paratiroidea ha evolucionado profundamente gracias al progreso de las técnicas de imagen. Hace veinte años, la exploración cervical quirúrgica era el único método que permitía identificar adenomas paratiroideos en más del 95% de los casos. Desde entonces, se practican ecografías de alta definición. La gammagrafía con Tc-99m sestamibi (MIBI) ayudó a detectar morfológica y funcionalmente los adenomas. La TAC también ha evolucionado. El departamento de ciencias informáticas del centro de formación IRCAD ha desarrollado un programa informático de imagen específico, que permite reconstruir virtualmente en tres dimensiones los diferentes órganos cervicales a partir de una simple TAC con inyección. La reconstrucción en 3D ayuda a localizar con precisión un adenoma paratiroideo en relación a las estructuras adyacentes, en particular las estructuras vasculares. Este vídeo ilustra perfectamente la ventaja de la reconstrucción en 3D, que permite corregir intraoperatoriamente la primera impresión. Enseguida se encuentra un primer adenoma pequeño, pero no corresponde a la imagen reconstruida, concretamente debido a su relación con la arteria tiroidea inferior. La disección de la región superior de la arteria, guiada por la reconstrucción en 3D, permite identificar el adenoma sospechado en el estudio de imagen. Las ventajas de esta técnica de imagen han permitido practicar exploraciones cervicales con un abordaje asistido por vídeo y la curación del paciente.
Strasbourg (FRANCE)
Profesor de Cirugía
Hospital Universitario de Estrasburgo, Francia

Strasbourg (FRANCE)
Cirujano Digestivo y Endocrino
Hospital Universitario de Estrasburgo, Francia


Profesores Expertos

Profesor de Cirugía
Università degli Studi di Pisa, Italy
Educación y formación
• 1972: Licenciado en Medicina y Cirugía por la Universidad de Pisa, Italia.
• 1976: Título de Especialista en Cirugía General por la Universidad de Pisa, Italia.
• 1978: Profesor Asociado de Cirugía de la Universidad de Pisa, Italia.
• 1986: Profesor Titular de Cirugía la Universidad de Pisa, Italia.
• 2002-2010: Director del Departamento de Cirugía de la Universidad de Pisa, Italia.
• 2006-2010: Vicerrector de la Universidad de Pisa, Italia, supervisión de las relaciones científicas con universidades de la CEE e internacionales.
Áreas de interés
Cirugía endocrina, cirugía tiroidea, cirugía paratiroidea, cirugía adrenal, cirugía mínimamente invasiva, cirugía endocrina robótica.

Profesora de Cirugía
Hospital Universitario de Estrasburgo
Educación y formación
- 1998: Licenciado en Medicina y Cirugía por la Universidad de Ancona, Italia
- 1998-2004: Residencia de Cirugía General, Universidad de Ancona, Italia
- 2000-2002: Médico Asistente de Investigación y Clínico del Departamento de Cirugía General de la UCSF San Francisco, EE. UU.
- 2004-2006: Asistente Clínico del Departamento de Cirugía General de la UCSF, San Francisco, EE. UU.
- 2007: Director del Laboratorio de Motilidad Esofágica y Fisiología Pélvica de la Universidad NHC, Estrasburgo, Francia
- 2007: Editor Asociado de la EATS (Asociación Europea de Cirugía Transluminal)
- 2010: Profesor de Cirugía del Hospital Universitario de Estrasburgo, Francia.
- 2012: Premio SAGES al desarrollo de la carrera
Áreas de interés
Cirugía GI superior con acceso mínimo (laparoscopia, endoscopia, cirugía guiada por la imagen), fisiología esofágica, cirugía bariátrica. El Dr. Perretta ha estado involucrado en los inicios de la experiencia clínica de la cirugía endoscópica transluminal a partir de orificios naturales (NOTES).

Profesor de Cirugía
Hospital Universitario de Estrasburgo, Francia
Educación y formación
• Presidente del IRCAD / EITS Instituto de Investigación del Cáncer Digestivo/ Instituto Europeo de Telecirugía.
• Presidente y miembro fundador de la Asociación Europea de Cirugía Transluminal, EATS.
• Editor Jefe de WeBSurg (Biblioteca Electrónica Internacional de Cirugía).
• Director y jefe del Departamento de Cirugía Digestiva y Endocrina, Hospital Universitario de Estrasburgo, Francia.
Áreas de interés
El Profesor Marescaux posee el reconocimiento internacional por su experiencia en cirugía mínimamente invasiva. Posee una amplia experiencia en cirugía endocrina y ha desarrollado técnicas quirúrgicas para enfermedades gastrointestinales. Fundó el Instituto de Investigación contra el Cáncer del Aparato Digestivo (IRCAD) y es Director del Instituto Europeo de Telecirugía (EITS), una escuela especializada que, anualmente, forma en cirugía laparoscópica a más de 3.000 cirujanos. En septiembre de 2001, el Profesor Marescaux llevó a cabo la primera intervención asistida por robot transatlántica, conocida como la Operación de Lindbergh. El 2 de abril de 2007, el Profesor Jacques Marescaux y su equipo llevaron a cabo con éxito la primera cirugía sin cicatriz. En su primera intervención quirúrgica sin incisión en humanos utilizó un endoscopio flexible en una colecistectomía transvaginal en una mujer de 30 años con litiasis biliar sintomática. Al principio, fue conocida mundialmente como la "operación Anubis". El Profesor Marescaux participa activamente en muchas asociaciones quirúrgicas, como el Royal College of Surgeons (Londres), la Asociación Quirúrgica Europea, la Academia Nacional de Medicina y la Sociedad Europea de Telemedicina.

Cirujano Digestivo y Endocrino
Hospital Universitario de Estrasburgo, Francia
Educación y formación
Desde 2000: Codirector científico del IRCAD/EITS (Instituto de Investigación contra el Cáncer del Aparato Digestivo/ Instituto Europeo de Telecirugía). Miembro del Consejo Editorial de WeBSurg (Biblioteca Electrónica Internacional de Cirugía).
Desde 1996: Cirujano consultor en el Hospital Universitario de Estrasburgo, Departamento de Cirugía de Urgencia, General y Endocrina.
Áreas de interés
El Dr. Vix posee una amplia experiencia en cirugía general y digestiva, y está especializado en cirugía de urgencia y de la obesidad mórbida. El Dr. Vix ha participado en el proyecto Estudio Experimental, Interfacial, Análisis, Rescate y seguimiento clínico de Implantes y Dispositivos Médicos, junto con el Profesor Stig Karlsson. Es miembro electo del Comité Médico del Hospital Universitario de Estrasburgo y miembro de varias asociaciones médicas, como la Asociación Francesa de Cirugía Endocrina y la Sociedad Francesa de Cirugía Digestiva.

Profesor de Cirugía Digestiva y Endocrina
Hospital Universitario de Estrasburgo, Francia
Educación y formación
• 1990: Licenciado en Medicina, Facultad de Medicina de Estrasburgo (Premio de Licenciatura), Francia
• 1990: Licenciado en Medicina, Especialista en Cirugía Digestiva
• 1995: Licenciado en Medicina, Especialista en Cirugía General
• 1996: Doctorado, Universidad Louis Pasteur, Estrasburgo, Francia
• 1999: Profesor de Cirugía, Universidad Louis Pasteur, Estrasburgo, Francia
• Desde 1992: Cirujano del Departamento de Cirugía Digestiva y Endocrina, Hospital Universitario de Estrasburgo, Francia
• Desde 1994: Vicepresidente del IRCAD/EITS (Instituto de Investigación contra el Cáncer del Aparato Digestivo / Instituto Europeo de Telecirugía)
Áreas de interés
El Prof. Mutter está muy interesado en las nuevas tecnologías, la era de la información y la robótica. Como cirujano, profesor e investigador, su objetivo es profundizar en el desarrollo de técnicas y en la práctica de la cirugía mínimamente invasiva, basada en cirugía guiada por la imagen, el modelado y la simulación médica y numérica, el uso de la robótica y la automatización.
Biblioteca Multimedia
Vídeos
Fotos
References
2. Franko J, Kish KJ, Pezzi CM, Pak H, Kukora JS. Safely increasing the efficiency of thyroidectomy using a new bipolar electrosealing device (LigaSure) versus conventional clamp-and-tie technique. Am Surg. 2006 Feb;72(2):132-6. PubMed
3. Fujita T, Doihara H, Ogasawara Y, Shimizu N. Utility of vessel-sealing systems in thyroid surgery. Acta Med Okayama. 2006 Apr;60(2):93-8. PubMed
4. Kirdak T, Korun N, Ozguc H. Use of ligasure in thyroidectomy procedures: Results of a prospective comparative study. World J Surg. 2005 Jun;29(6):771-4. PubMed
5. Lepner U, Vaasna T. Ligasure vessel sealing system versus conventional vessel ligation in thyroidectomy. Scand J Surg. 2007;96(1):31-4. PubMed
Agradecimientos
Todo el equipo de WeBSurg quiere expresar su afectuoso agradecimiento por su innovador trabajo a todos los cirujanos que han contribuido activamente en este proyecto, en particular al Dr. Michel Vix, la Dra. Silvana Perretta y el Profesor Didier Mutter. Un agradecimiento especial para el Profesor Paolo Miccoli, por su importante contribución en este módulo de e-learning.
También queremos dar las gracias a Covidien, fabricante y suministrador del sistema LigaSure™ Small Jaw Instrument, por hacer posible el desarrollo de este manual de e-learning.
Queremos felicitar a Donna S. Watson (Directora de Desarrollo Curricular del Curso de Covidien) y a Fiona Morrison (Directora Principal, Soluciones Quirúrgicas Globales PACE de Covidien) que amablemente han respondido a todas nuestras preguntas acerca de LigaSure™ Small Jaw Instrument, y que nos han ayudado a ensamblar el módulo de e-learning. Finalmente, agradecemos el constante apoyo y el gran talento del Profesor Jacques Marescaux.
Créditos
Este módulo de e-learning ha sido concienzudamente ilustrado por Catherine Cers, ilustradora médica.
Del diseño gráfico se ha encargado Gaelle Lechner-Giovannoni.
Las fotografías las ha proporcionado Julie Duffet; la edición de las secuencias Melody Meyer di Rosa, Thibaud Balland, David Hiltenbrand y Carlos Alves, técnicos de audiovisuales.
Del desarrollo se han ocupado Nicolas Hirlemann y Stephane Becker, creadores de sitios Web.
La revisión lingüística y las traducciones han estado a cargo de Christopher Burel y Guy Temporal, revisores médicos.
El desarrollo del producto lo ha realizado Thomas Parent, Director Técnico de WeBSurg.

 Español ▼
Español ▼ English
English Français
Français Deutsch
Deutsch Italiano
Italiano Portuguese
Portuguese 简体中文
简体中文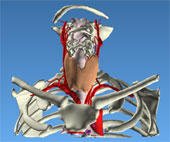
 Fuentes de energía
Fuentes de energía Opiniones de los expertos
Opiniones de los expertos Intervención quirúrgica
Intervención quirúrgica Clinical Experience Using Multifunctional LigaSure™ Small Jaw
Clinical Experience Using Multifunctional LigaSure™ Small Jaw LigaSure™ Small Jaws Instrument
LigaSure™ Small Jaws Instrument LigaSure™ Small Jaws brochure
LigaSure™ Small Jaws brochure Self-study guide Electrosurgery
Self-study guide Electrosurgery